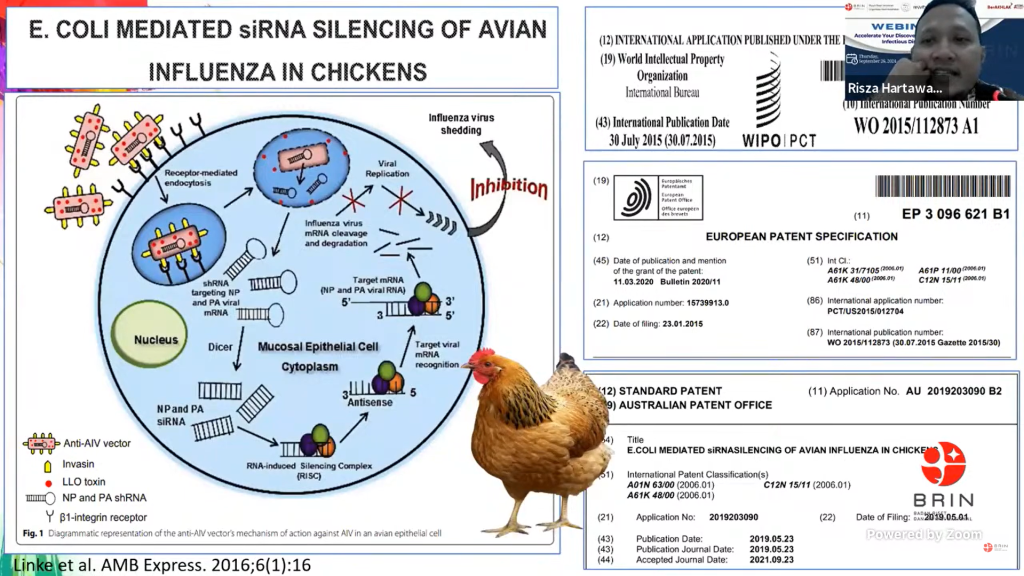
Dengan pemahaman mendalam terhadap biologi virus dan mekanisme RNAi, maka bisa dirancang terapi yang lebih presisi dan efektif
Di tengah meningkatnya ancaman penyakit infeksi akibat virus, upaya pencarian terapi baru terus dilakukan melalui pendekatan ilmiah yang lebih presisi dan berbasis molekuler. Salah satu pendekatan inovatif yang kini mendapat perhatian adalah pemanfaatan mekanisme epigenetik, khususnya melalui RNA interference (RNAi), dalam pengembangan antiviral. Pendekatan ini tidak hanya menawarkan cara kerja yang berbeda dari obat konvensional, tetapi juga membuka peluang besar untuk terapi yang lebih spesifik, efektif, dan minim efek samping, menjadikannya sorotan penting dalam studi bioteknologi modern.
Dalam pemaparannya, Peneliti Pusat Riset Veteriner, Organisasi Riset Kesehatan, Badan Riset dan Inovasi Nasional (BRIN), Risza Hartawan, menjelaskan bahwa pendekatan ini termasuk dalam studi epigenetik, yaitu perubahan ekspresi genetik yang tidak disebabkan oleh modifikasi urutan DNA (Asam Deoksiribonukleat) itu sendiri. Mekanisme ini memungkinkan ekspresi gen diaktifkan atau dimatikan tanpa merubah kode dasar DNA.
Risza mengawali dengan menguraikan sentral dogma biologi, yaitu alur informasi genetik dari DNA menjadi RNA (Asam Ribonukleat) lalu diterjemahkan menjadi protein. Namun, ada regulasi tambahan yang tidak tergantung dari urutan basa DNA. Salah satunya adalah melalui RNA non-koding seperti small interfering RNA (siRNA) dan microRNA (miRNA), yang dahulu dianggap ‘sampah’ namun ternyata sangat krusial dalam proses biologis.
“siRNA dan miRNA sama-sama berperan dalam menekan ekspresi gen, meskipun mekanismenya berbeda. siRNA biasanya berasal dari luar tubuh dan bekerja dengan mengenali pasangan mRNA (RNA pembawa pesan) secara sempurna untuk kemudian mendegradasinya. Sementara itu, miRNA bersifat endogen, mengenali mRNA secara parsial, dan menghambat translasi atau menyebabkan degradasi tidak langsung terhadap mRNA target,” jelas dia.
Menurut Risza, perbedaan utama antara keduanya terletak pada tingkat spesifisitasnya. siRNA bekerja sangat spesifik dengan memotong langsung mRNA target, sedangkan miRNA lebih fleksibel tetapi bisa menarget banyak gen sekaligus. Keduanya memiliki potensi besar sebagai terapi, termasuk untuk penyakit infeksi dan kanker.
Dalam konteks penyakit menular, ia melanjutkan, RNAi telah banyak diterapkan dalam penelitian terhadap virus influenza, yang dikenal sangat mudah bermutasi dan pernah menimbulkan pandemi. “Sejak 2003, riset telah difokuskan pada penargetan gen penting seperti nukleoprotein virus. Namun karena virus terus bermutasi, siRNA yang efektif untuk satu subtype belum tentu bekerja untuk subtype lainnya,” ujarnya.
Aplikasi RNAi sebagai Antiviral
Rizsa memberi contoh salah satu penggunaan miRNA, yakni microRNA-24 yang telah terbukti mampu menurunkan ekspresi protein furin. Furin berperan dalam aktivasi hemaglutinin pada virus influenza, sebuah langkah penting dalam proses infeksi. Penurunan konsentrasi miR-24 menyebabkan peningkatan aktivitas furin, dan sebaliknya.
“Dalam percobaan, penambahan miR-24 sintetis dapat menekan aktivitas furin dan dengan demikian bisa menurunkan tingkat infeksi. Namun, efek ini tidak berlaku pada semua varian virus, karena mekanisme aktivasi hemaglutinin bisa berbeda. Pada varian H5N1 misalnya, furin sangat penting, tapi pada H1N1 tidak,” jelas dia.
Risza juga memaparkan, penelitian yang berhasil mengidentifikasi beberapa miRNA seperti miR-431, miR-744, dan miR-205 mampu menekan ekspresi protein nukleoprotein influenza. Dengan menambahkan miRNA sintetis yang menyerupai ketiga miRNA tersebut, ekspresi protein virus dapat ditekan secara signifikan.
Selengkapnya Baca di Majalah TROBOS Livestock edisi 310/ Juli 2025